
近日,来自中山大学生命科学学院的研究团队在国际知名期刊《Advanced Science》发表了题为“HMGB2-RAD21 Axis Promotes Fibro/Adipogenic Progenitor Proliferation and Regulates Fat Infiltration”的研究论文。该研究首次系统阐明了HMGB2通过转录激活RAD21调控纤维/脂肪祖细胞(FAPs)增殖的分子机制,为理解肌肉脂肪沉积的发育起源提供了新视角,也为猪肉品质改良和肌肉脂肪相关疾病治疗提供了潜在靶点。
肌肉脂肪的形成始于出生后,但数量决定在胚胎期
肌肉内脂肪含量是影响猪肉品质的关键因素,也与多种肌肉疾病密切相关。纤维/脂肪祖细胞是肌肉中脂肪细胞的主要来源。
研究团队利用高肌肉脂肪含量的广东小耳花猪模型,收集了从胚胎期到成年期多个时间点的背最长肌样本,通过组织染色发现:肌肉脂肪细胞最早在出生后第2天才出现,之后逐渐增多(图1B、1C)。
然而,转录组分析提示,脂肪分化的“准备”工作早在胚胎晚期就已启动(图1F、1G)。
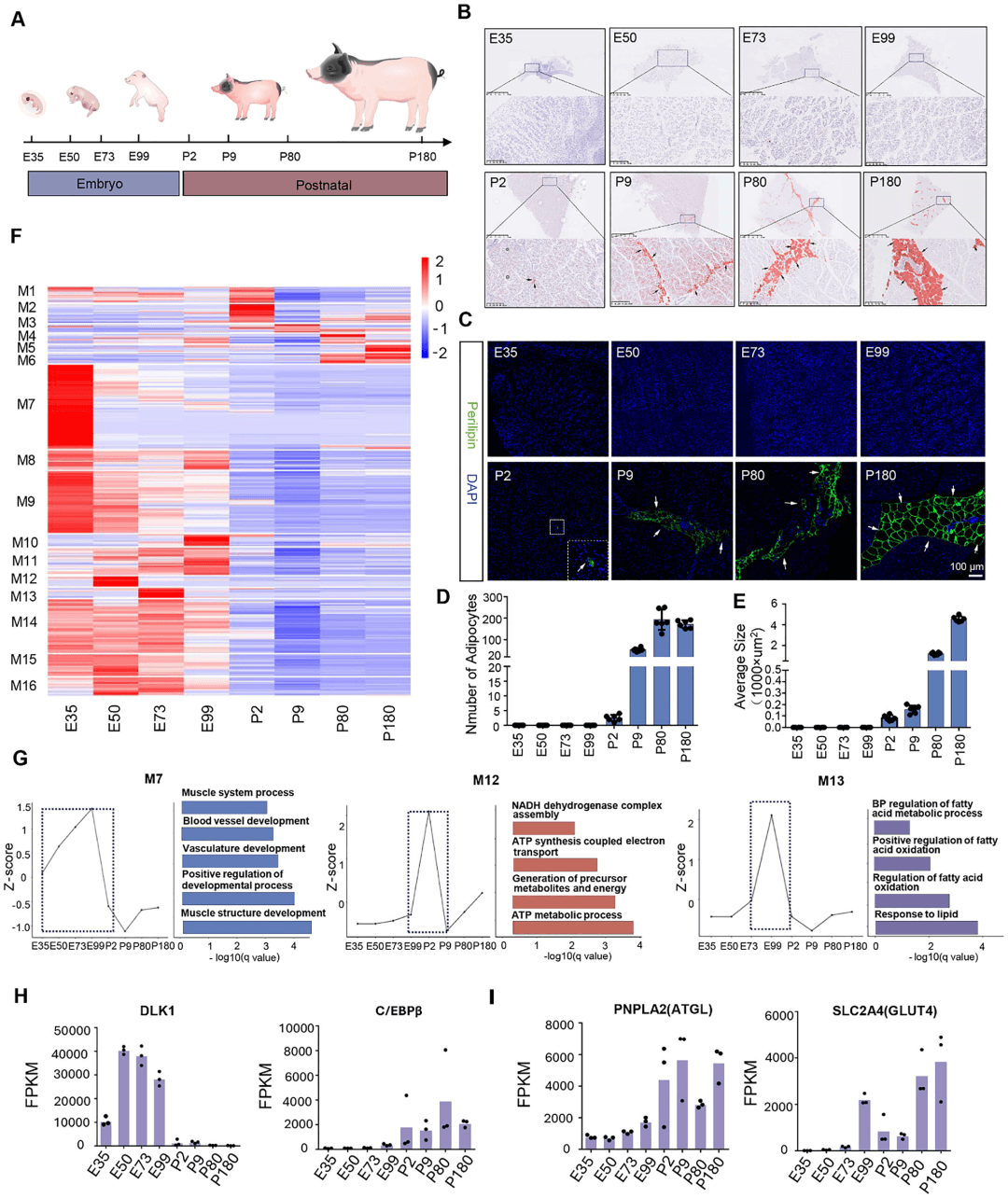
图1 骨骼肌肌间脂肪细胞分化的时间动态
(A)收集广东小耳花猪在八个发育时间点的背最长肌样本:胚胎日(E)和出生后日(P)。
(B)不同发育阶段背最长肌样本的油红O染色。
(C)不同发育阶段背最长肌样本的Perilipin免疫荧光染色。
(D)肌间脂肪细胞数量的定量分析。
(E)肌间脂肪细胞大小的定量分析。
(F)热图显示16个共表达模块中基因的表达模式(每个发育阶段包含三个生物学重复)。
(G)模块7、12和13的表达变化及GO富集分析。左侧面板显示每个模块基因在骨骼肌发育过程中的中位数Z评分,右侧面板列出与每个模块相关的前五个或四个典型GO生物学过程条目。
(H、I)葡萄糖代谢相关基因 (GLUT4)和脂肪生成相关基因(DLK1、C/EBPβ和ATGL)在骨骼肌发育过程中的FPKM水平变化。
单细胞图谱揭示FAPs^HMGB2+ 亚群是关键增殖群体
为进一步探究FAPs的发育起源,团队对胚胎期和新生期猪肌肉组织进行了单细胞RNA测序,构建了首个猪胚胎期FAPs发育图谱(图2A)。通过无监督聚类和拟时序分析,研究者发现一个高表达HMGB2的FAP亚群(FAPs^HMGB2+)主要处于活跃增殖状态(图2C、2D),位于分化轨迹的起点(图2G),之后分化为成脂和成胶原两个方向(图2J、2K)。
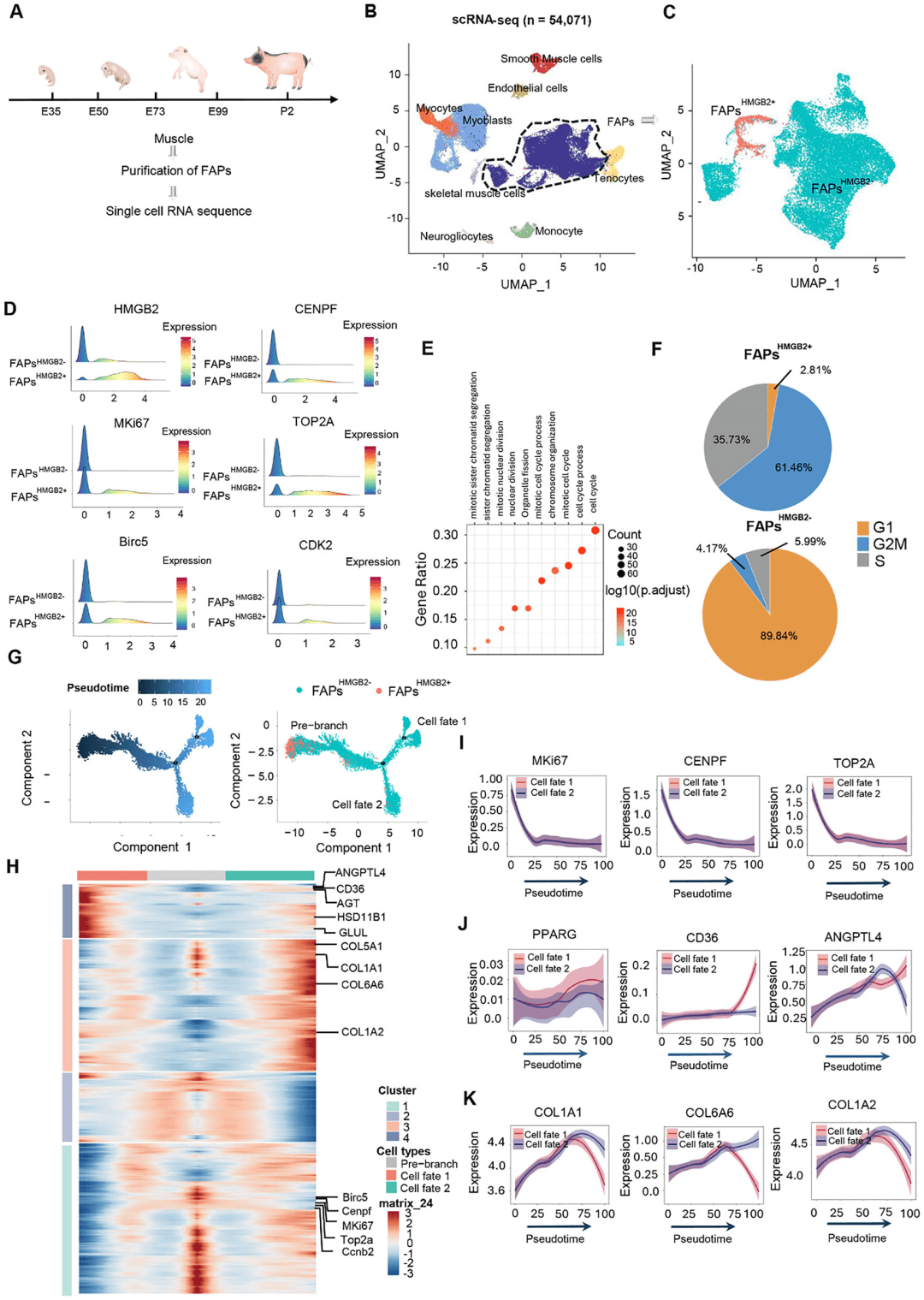
图2 胚胎骨骼肌发育过程中FAPs亚群的发育轨迹
(A)猪肌肉组织准备、单细胞分离及单细胞RNA测序流程示意图。
(B)基于图的聚类分析显示分离的单细胞形成代表不同细胞群的独立聚类。
(C)基于图的聚类分析显示FAPs群体中存在两个不同的亚群:FAPs^HMGB2- 和 FAPs^HMGB2+。
(D)FAPs^HMGB2+ 亚群中代表性基因的表达情况。
(E)FAPs^HMGB2+ 亚群高表达基因的GO富集分析。
(F)不同FAPs亚群中各细胞周期时相的比例。
(G)通过Monocle 2对FAPs进行拟时序分析,揭示三种不同的细胞状态:前分支状态、细胞命运1和细胞命运2。细胞状态的分布沿拟时序轨迹呈现,每个点代表一个细胞。
(H)热图显示按拟时序排列的3941个主要差异表达基因的表达变化,这些基因被划分为四个呈现不同表达模式的主要簇。
(I)增殖相关基因(如Ki67、CENPF和Top2A)的动态表达。
(J、K)成脂和成胶原相关基因的动态表达。
FAPs^HMGB2+亚群的比例随发育进程逐渐下降,至出生后几乎消失(图3A-3D),提示胚胎期FAPs的增殖活性直接决定了出生后FAPs库的大小,进而影响肌肉脂肪的沉积潜力。
免疫荧光染色进一步证实,FAPs^HMGB2+细胞在早期胚胎阶段(E35)呈现Ki67阳性,表明其正处于活跃增殖状态(图3G、3H)。
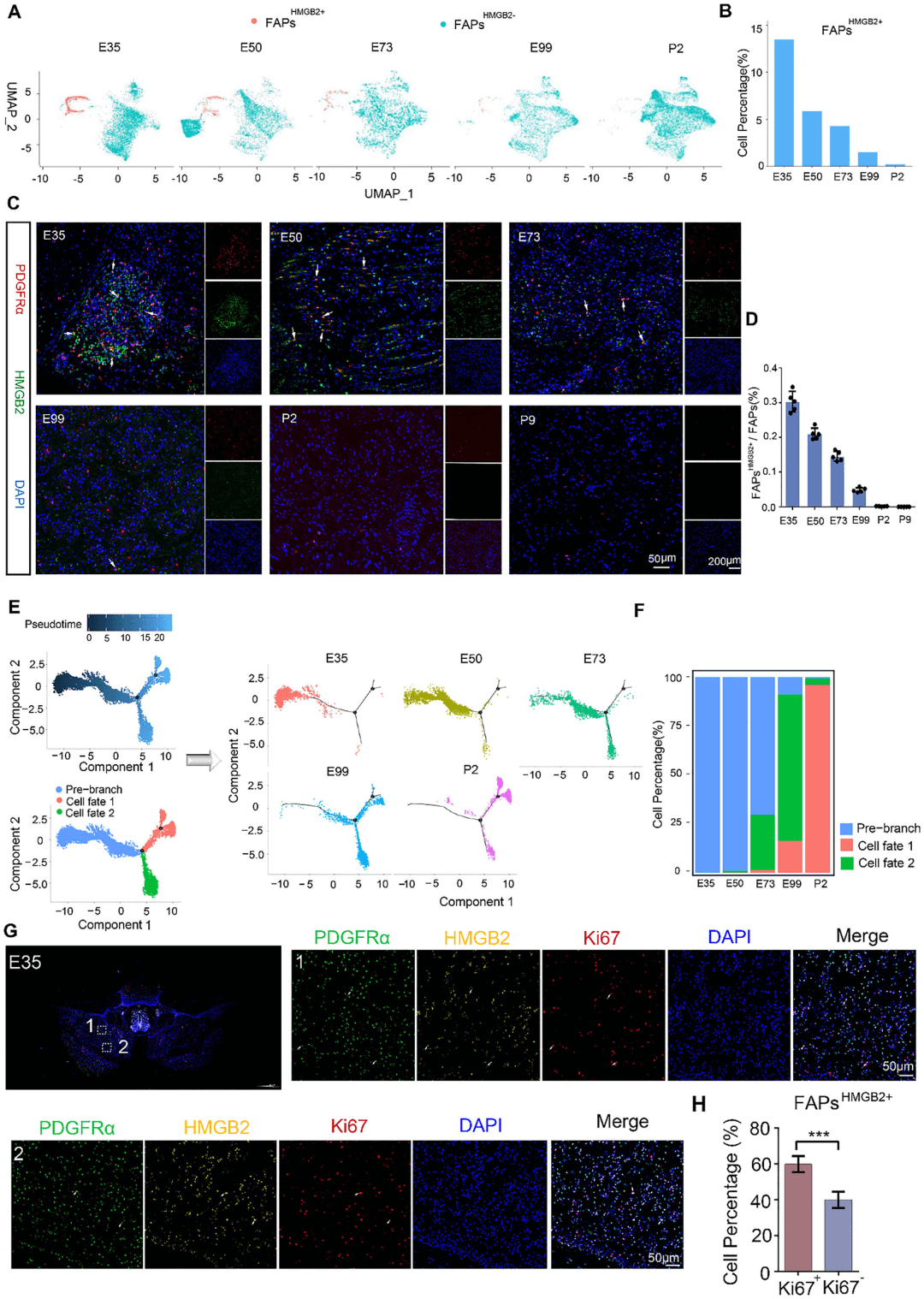
图3 FAPs^HMGB2+ 在猪骨骼肌发育的胚胎阶段占主导地位
(A)UMAP图显示不同发育阶段骨骼肌中FAPs亚群的分布。
(B)各发育阶段FAPs^HMGB2+ 占FAPs总数的比例。
(C和D)对GDSS猪在E35、E50、E73、E99、P2和P9时期的背肌横断面石蜡切片进行HMGB2和PDGFRα免疫荧光共染,并对FAPs中FAPs^HMGB2+ 的比例进行定量分析。
(E)不同发育阶段FAPs分化轨迹的可视化。
(F)各发育阶段骨骼肌中处于三种细胞状态(前分支、细胞命运1和细胞命运2)的FAPs比例。
(G)对早期骨骼肌样本(E35)进行PDGFRα、HMGB2和Ki67的多重免疫荧光染色。
(H)对早期骨骼肌样本(E35)中FAPs^HMGB2+ 群体内Ki67阳性细胞的比例进行定量分析。
HMGB2敲除导致FAPs减少,脂肪浸润能力下降
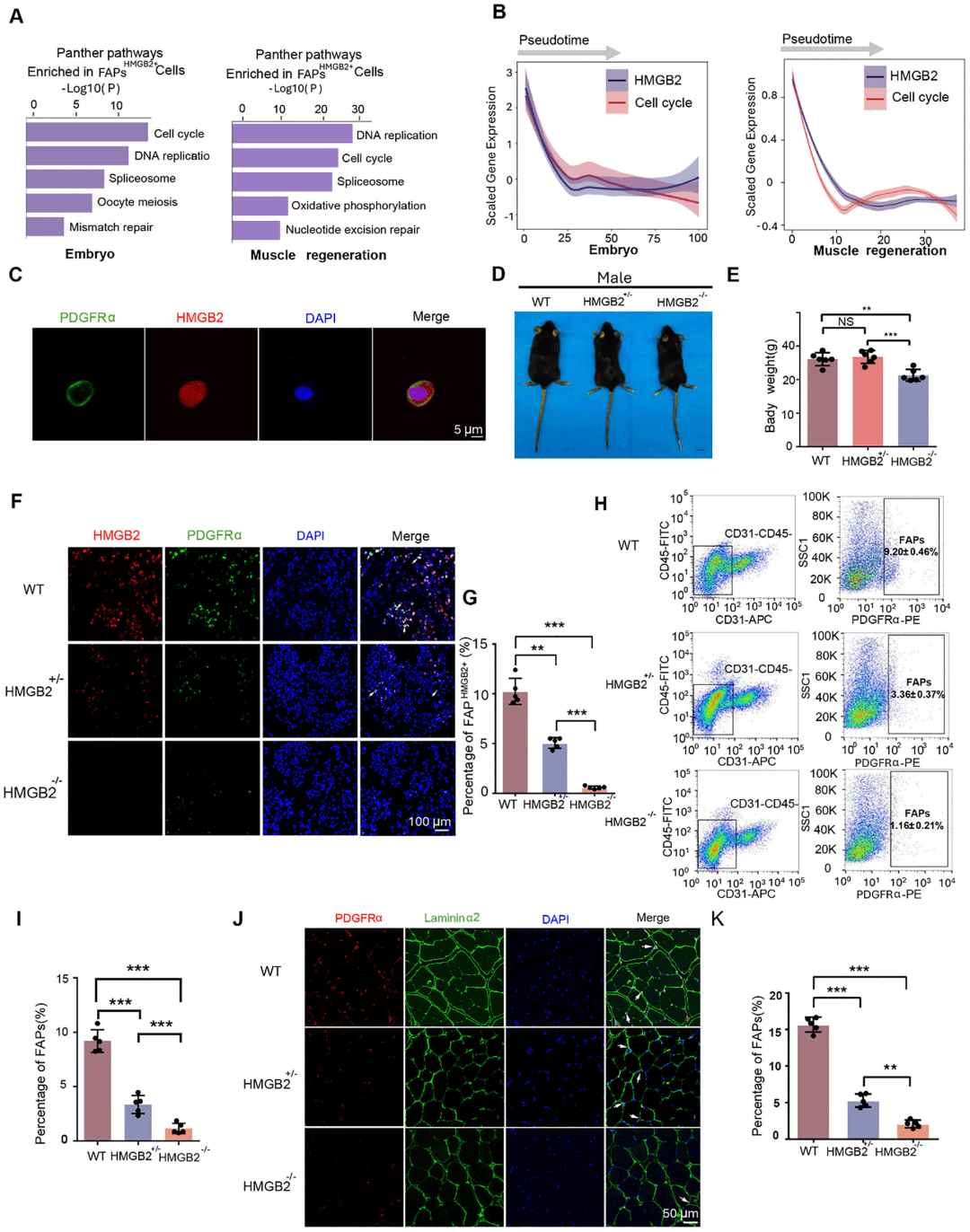
图5 HMGB2调控FAPs的增殖能力
(A)对胚胎发育和肌肉损伤过程中FAPs^HMGB2+ 的KEGG通路分析。
(B)HMGB2表达与细胞周期通路的变化趋势。
(C)体外培养的小鼠FAPs(CD31-CD45-PDGFRα+)中PDGFRα和HMGB2的免疫荧光共染。
(D)8周龄对照、HMGB2+/− 和 HMGB2−/− 雄性小鼠的代表性图像。比例尺 = 1 cm。
(E)8周龄不同基因型雄性小鼠的体重(每种基因型 n = 6)。
(F)胚胎第14天(E14)肌肉中HMGB2和PDGFRα的免疫荧光共染。
(G)不同基因型中FAPs^HMGB2+ 的比例。
(H)通过流式细胞术对8周龄不同基因型小鼠胫骨前肌中FAPs进行定量分析。
(I)8周龄不同基因型小鼠胫骨前肌中FAPs的比例。
(J)基于免疫荧光染色鉴定8周龄不同基因型小鼠胫骨前肌中的FAPs含量。
(K)FAPs含量的定量分析。
在肌肉损伤模型中,HMGB2敲除小鼠的肌肉脂肪浸润能力显著减弱(图6A-6D)。在衰老模型中也观察到类似趋势(图6E、6F),同时肌肉纤维化程度也明显降低(图6G、6H),表明HMGB2是调控FAPs增殖和脂肪沉积能力的关键分子。
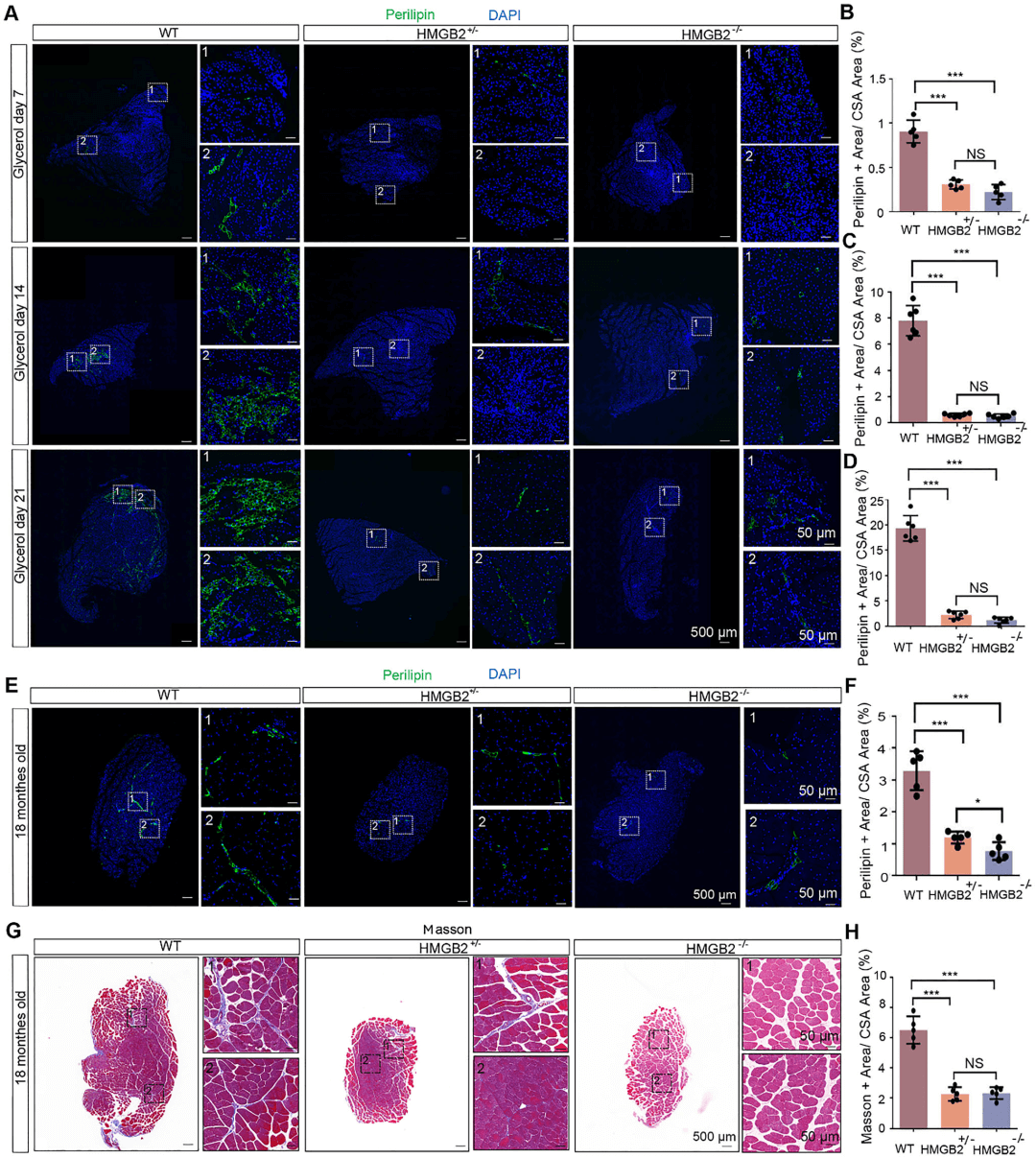
图6 骨骼肌中FAPs减少对肌肉损伤和衰老的影响
(A)通过Perilipin免疫荧光染色检测野生型、HMGB2+/− 和 HMGB2−/− 小鼠在甘油损伤后第7、14和21天骨骼肌中的脂肪浸润情况。
(B)损伤后第7天肌肉横切面中Perilipin阳性区域的定量分析(n = 3)。
(C)损伤后第14天肌肉横切面中Perilipin阳性区域的定量分析(n = 3)。
(D)损伤后第21天肌肉横切面中Perilipin阳性区域的定量分析(n = 3)。
(E)通过Perilipin免疫荧光染色评估16月龄小鼠骨骼肌中的脂肪浸润情况。
(F)衰老模型肌肉横切面中Perilipin阳性区域的百分比(n = 3)。
(G)通过Masson染色评估肌肉中的胶原沉积情况(衰老模型,16月龄)。
(H)衰老模型肌肉横切面中Masson阳性区域的百分比(n = 3)。
机制解析:HMGB2直接激活RAD21转录
在机制层面,研究者发现HMGB2通过结合RAD21启动子区域(图8L),直接激活其转录。ChIP-qPCR实验证实HMGB2在RAD21启动子上显著富集(图8M)。RAD21是黏连蛋白复合物的核心亚基,参与DNA复制和细胞周期调控。
体外敲低HMGB2或RAD21均导致FAPs增殖能力下降(图8B-8G),而过表达RAD21可部分挽救HMGB2敲低引起的增殖缺陷(图8H-8K)。这一HMGB2-RAD21轴的发现,为理解FAPs增殖的转录调控网络提供了新线索。
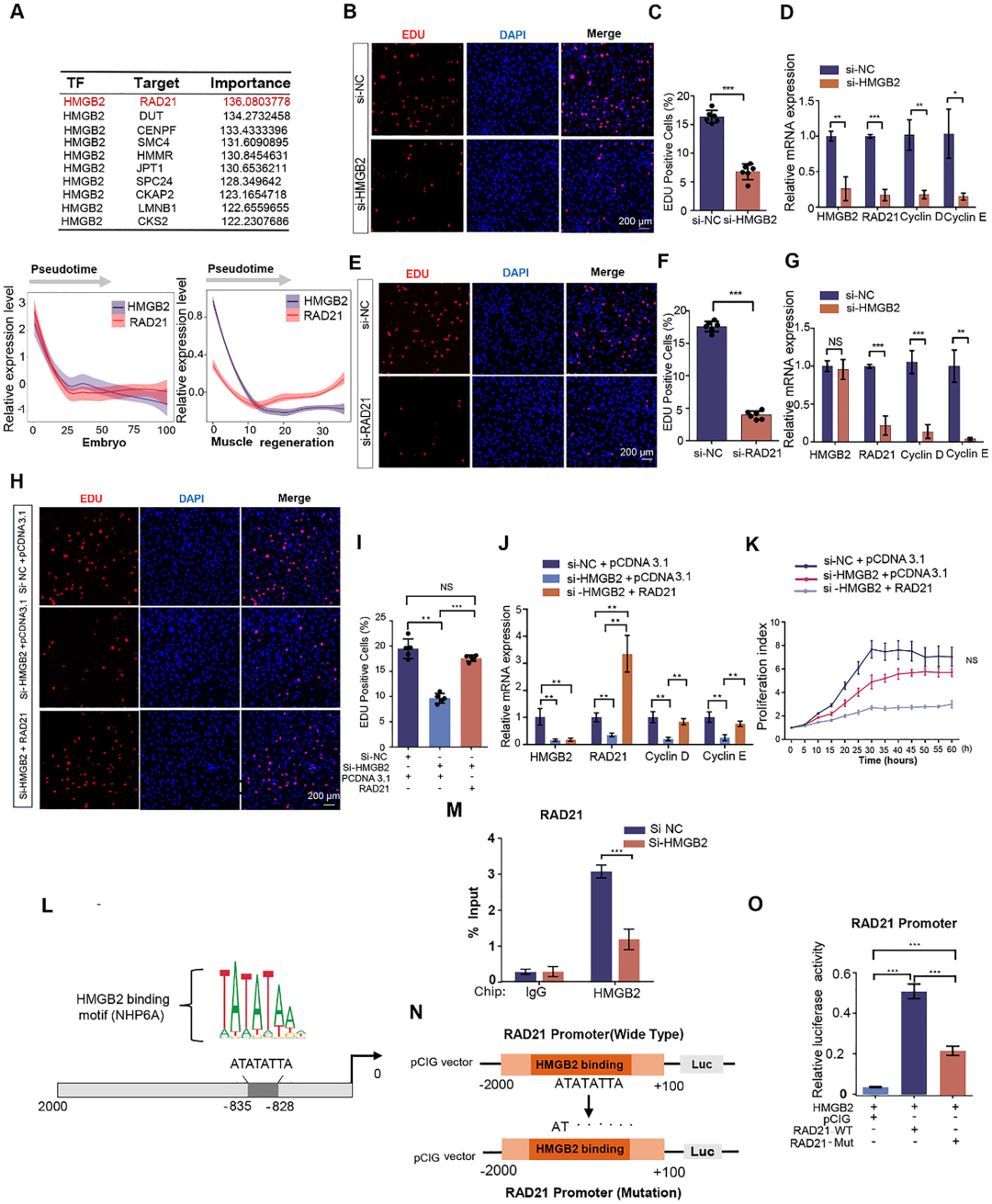
图8 HMGB2直接结合RAD21启动子并激活其转录
(A)HMGB2和RAD21在FAPs发育轨迹中的表达趋势。
(B、C)转染si-HMGB2后小鼠FAPs的EDU染色。
(D)转染si-HMGB2后通过qPCR检测HMGB2、RAD21、Cyclin E1和Cyclin D1的mRNA水平(n = 3)。
(E、F)转染si-RAD21后小鼠FAPs的EDU染色。
(G)转染si-RAD21后通过qPCR检测HMGB2、RAD21、Cyclin E1和Cyclin D1的mRNA水平(n = 3)。
(H)转染si-HMGB2和pCDNA3.1-RAD21后小鼠FAPs的EDU染色。
(I)EDU阳性细胞的定量分析。
(J)通过qPCR检测HMGB2、RAD21、Cyclin E1和Cyclin D1的mRNA水平(n = 3)。
(K)FAPs的实时增殖指数。
(L)使用JASPAR数据库预测RAD21启动子区域(-2000至+0 bp)内的HMGB2结合位点。
(M)通过ChIP-qPCR分析对照细胞和KLF4敲低细胞中HMGB2在RAD21启动子上的富集情况。数据标准化为输入样本的百分比。
(N)实验设计示意图:扩增RAD21启动子序列(-2000至+0 bp),删除预测的结合区域"ATATTA",并插入携带萤火虫荧光素酶和海肾荧光素酶的双荧光素酶报告载体pCIG中。
(O)在293T细胞中进行的双荧光素酶报告基因检测,细胞共转染含有野生型或突变型RAD21启动子的报告质粒和pCDNA3.1-HMGB2载体(n = 3)。
研究意义与展望
该研究首次从发育生物学角度阐明了肌肉脂肪沉积的细胞起源和分子调控机制,不仅为猪的分子育种提供了新的候选基因,也为肌营养不良、2型糖尿病等疾病中的病理性脂肪浸润干预提供了潜在靶点。研究团队表示,后续将进一步探索FAPs特异性调控策略,以期在改善肉质和治疗肌肉疾病之间找到平衡点。
原文链接:https://doi.org/10.1002/advs.202514363
研究背后的实验保障
在整个研究过程中,精准的基因表达分析是验证机制的关键环节。
研究团队使用了东盛生物GDSBio的SYBR Green qPCR Mix(P2091/P2092/P2093/P2094),在罗氏LightCycler 480 II系统上完成了实时荧光定量PCR检测,包括基因敲除小鼠模型的验证、siRNA干扰效率的评估、ChIP-qPCR中对低丰度DNA模板的精确定量,为研究数据的可靠性提供了坚实保障。

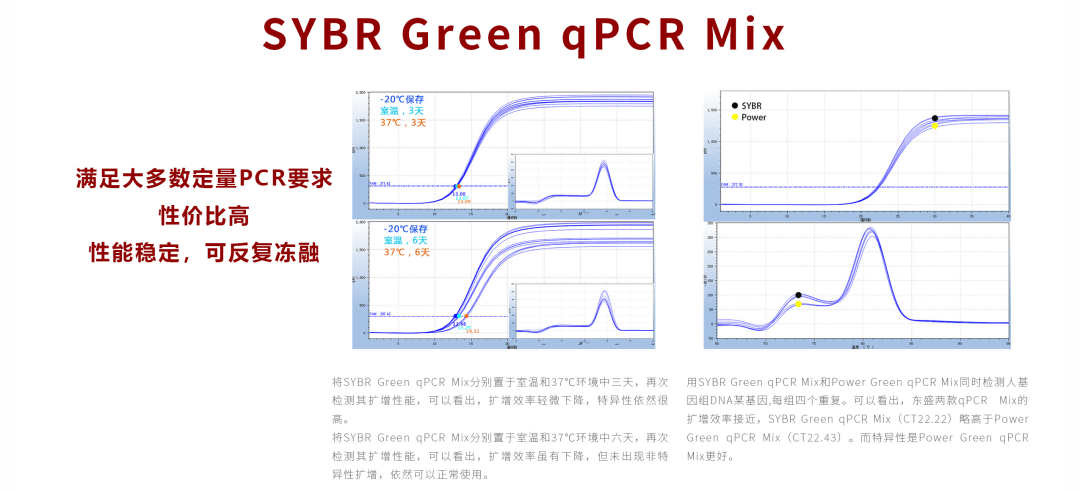
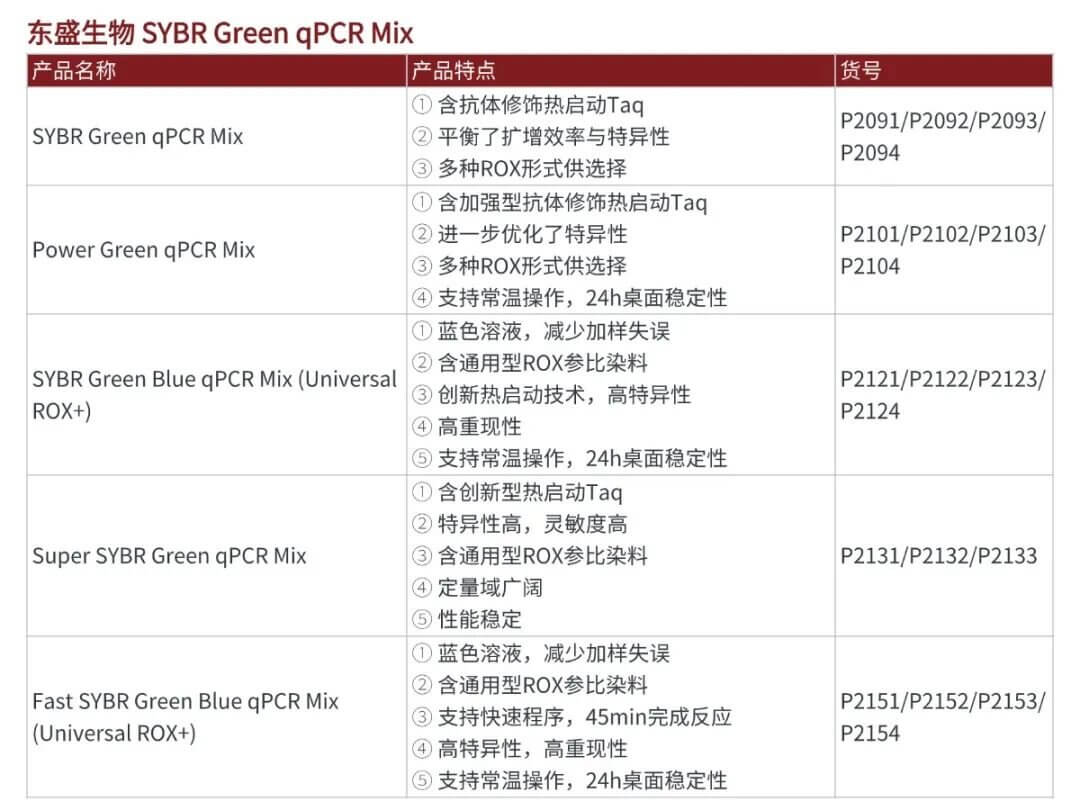
SYBR Green qPCR Mix系列是东盛生物经典的染料法荧光定量PCR预混液,经过长期的市场检验及持续的改进优化,产品性能优异,质量稳定,拥有众多海内外稳定用户。同时,该系列依据ROX参比染料提供形式的不同有多种规格供选择:
#P2091 SYBR Green qPCR Mix (NO ROX):不含ROX
#P2091a SYBR Green qPCR Mix (Low ROX+):预混低浓度ROX
#P209b SYBR Green qPCR Mix (High ROX+):预混高浓度ROX
#P2091c SYBR Green qPCR Mix (with ROX+):独立包装ROX
产品支持免费试用,同时有多种选择,满足不同的使用需求。
45分钟革新:qPCR进入“高速时代”
订购咨询
广州东盛生物科技有限公司
📧 sales@gdsbio.com
📞 020-87791356
🌐 www.gdsbio.cn
